Spirti
D.Cēdere. Spirti
4. Alkanolu fizikālās īpašības
Zemākie alkanoli (līdz C12) istabas temperatūrā ir bezkrāsaini šķidrumi, tālākie alkanoli ir bezkrāsainas, cietas vielas. To blīvums ir mazāks par 1 g/ml.
Alkanolu viršanas temperatūras ir daudz augstākas nekā alkāniem ar tādu pašu molekulmasu. Paaugstināto viršanas temperatūru cēlonis ir saites O-H polaritāte. Tā rezultātā starp alkanola molekulām veidojas ūdeņraža saites un norisinās šo molekulu asociācija. Starpmolekulārās ūdeņraža saites var konstatēt spektroskopiski un ar rentgenstruktūranalīzi. Attālums starp blakusesošo molekulu skābekļa atomiem ir aptuveni 0,28 nm. Ja pieņemtu, ka asociācija nenorisinās, tad šim attālumam būtu jābūt lielākam (0,35 nm):
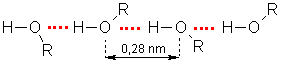
Šķidrumam iztvaikojot, ūdeņraža saites starp molekulām pārtrūkst. Šim procesam jāpatērē papildu enerģija, tāpēc arī viršana notiek augstākā temperatūrā nekā alkāniem.Homologu rindā, pieaugot molekulmasai, alkanolu viršanas temperatūras paaugstinās līdzīgi kā alkāniem. Alkanoliem ar sazarotu oglekļa atomu virkni viršanas temperatūras ir zemākas nekā alkanoliem ar nesazarotu virkni.
Alkanolu molekulas var veidot ūdeņraža saites ne tikai savā starpā, bet arī ar ūdens molekulām:
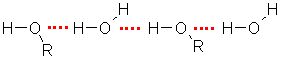
Tāpēc zemākie alkanoli labi šķīst ūdenī. Metanols un etanols sajaucas ar ūdeni jebkurās attiecībās. Spirta molekulu nosacīti var sadalīt divās daļās. Ogļūdeņraža atlikums (alkilgrupa) ir hidrofobā daļa, bet hidroksilgrupa - hidrofilā daļa. Ūdeņraža saišu veidošanos ar ūdens molekulām un tātad arī šķīdību ūdenī nodrošina hidroksilgrupa. Palielinoties ogļūdeņraža atlikumam, spirta šķīdība ūdenī samazinās:
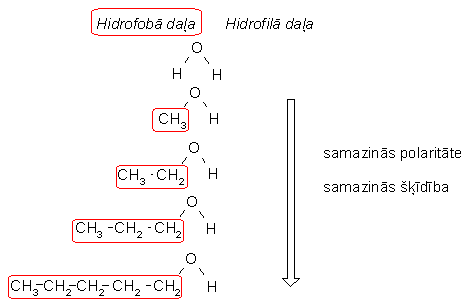
Alkanoli ir labi šķīdinātāji. Polārās -OH grupas dēļ alkanolos šķīst polāras vielas, bet nepolārais ogļūdeņraža atlikums nodrošina nepolāru vielu šķīdību. Tāpēc, piemēram, etanolā šķīst gan ūdens, gan benzols.